GIANT CRANIOPHARYNGIOMA – TRANSNASAL ENDOSCOPIC APPROACH
Rezumat:
Craniofaringioamele au avut încă de la începuturi un loc proeminent în neurochirurgie, atât datorită dificultății tehnice a rezecției lor, cât și a controverselor privind tratamentul optim al acestor tumori benigne. Harvey Cushing a descris în 1936 craniofaringioamele drept „cea mai inaccesibila dintre tumorile intracraniene”. 70 de ani mai târziu, Rutka încă mai scria: „Nu există altă tumoare cerebrală primară care să evoce mai multă pasiune, emoție și, prin urmare, controverse decât craniofaringiomul.”
Tehnicile de chirurgie endoscopică au avansat semnificativ în ultimele două decenii. Chirurgia endoscopică transnazală transsfenoidală oferă o vizualizare mai bună a câmpului operator în comparație cu chirurgia microscopică și are avantajul unei morbidități mai mici decât în cazul altor tehnici.
Cuvinte cheie: craniofaringiom, chirurgie endoscopică transsfenoidală
Abstract:
Craniopharyngiomas have had a prominent place in neurosurgery due to both the technical difficulty and controversy regarding the optimal treatment of these benign tumors. Harvey Cushing famously described craniopharyngiomas in 1936 as “the most forbidding of the intracranial tumors.” Seventy years later, Rutka still wrote: “There is no other primary brain tumor that evokes more passion, emotion, and as a result, controversy than does the CP.”
Endoscopic surgery techniques had been advancing in these last two decades. Transsphenoidal approach endoscopic surgery to the skull base provides better visualization of the operation field compared to microscopic surgery, and also brings lower morbidity than other techniques.
Keywords: craniopharyngioma, transsphenoidal endoscopic surgery
Craniofaringiomul este o tumoare benignă care derivă din rămășițele pungii lui Rathke. Este considerată pe scară largă a fi una dintre cele mai dificile tumori intracraniene. Craniofaringioamele cuprind 1-2% dintre toate tumorile cerebrale, 40% dintre cazuri apar între 5-15 ani și 60% apar la vârste > 55 de ani. Diagnosticul diferențial pentru craniofaringiom poate include o varietate de entități, inclusiv macroadenomul hipofizar, cordom, gliom, meningiom, disgerminom sau metastaze. Caracteristicile imagistice includ de obicei o leziune chistică, împroșcată cu calcificări la 50-80% dintre tumori (în special în cazuistica pediatrică), sunt tumori cu creștere lentă și pot ocupa regiunea selară și paraselară.
Frecvent pacienții asociază hipopituitarism și diabet insipid. Pacienții pot rămâne asimptomatici mult timp, manifestările clinice debutează frecvent cu tulburari de vedere sau dureri de cap.
Tratamentul de elecție este cel chirurgical. În mod tradițional, craniofaringioamele erau abordate neurochirurgical transcranian, dar dezvoltarea chirurgiei endoscopice transnazale transsfenoidale a permis în ultimii 20 de ani un abord minim invaziv endoscopic în condiții de siguranță, în echipă mixtă neurochirurgie – ORL. Dilema îndepărtării radicale a craniofaringioamelor constă în conservarea hipotalamusului și a tijei hipofizare versus recidiva tumorală. Abordarea endonazală endoscopică pentru rezecția craniofaringiomului oferă o vedere largă a câmpului operator și observarea directă a hipotalamusului și a originii tumorii. În literatura de specialitate clasificarea modernă divizează aceste tumori în 2 tipuri: periferice și centrale, în funcție de relația cu tija hipofizară (Bin Tang, Nature/ Scientific Reports, 2018) .
Tipul central (29% dintre toate craniofaringioamele) crește în interiorul și de-a lungul tijei pituitare și este situat strict pe linia mediană. În aceste cazuri tija hipofizară este greu de prezervat intraoperator (cu succes doar în 15% dintre cazuri).
Tipul periferic a fost împărțit în continuare în 3 subtipuri: subtipul dezvoltat din porțiunea hipotalamică a tijei, din tija supraselară sau din tija intraselară, în funcție de locul de origine diferit de-a lungul axei hipotalamo-hipofizare.
Tipul periferic apare din tijă, dar se extinde și crește lateral într-un model exofitic, reprezentând 71% dintre toate craniofaringioamele. În aceste cazuri, în centrele chirurgicale consacrate, rata de conservare postoperatorie a tijei este de aproximativ 75%.
Craniofaringioamele provenite din tija hipotalamică (cca 55% dintre tumorile periferice) se dezvoltă la joncțiunea hipotalamusului cu tija hipofizară. În aceste tumori, postchirurgical constatăm în toate cazurile apariția unor leziuni hipotalamice.
Craniofaringioamele tijei supraselare (20% dintre tumori) provin din porțiunea inferioara a tijei și deplasează hipotalamusul cranial, foarte rar îl infiltrează.
Craniofaringioamele tijei intraselare (25% dintre tumorile periferice) apar din regiunea subdiafragmatică a tijei și nu lezează de obicei hipotalamusul.
Recunoașterea originii craniofaringiomului este utilă pentru a înțelege modelul său de creștere și relația cu hipotalamusul, care sunt esențiale în planificarea celei mai adecvate abordări chirurgicale și gradul de rezecție.
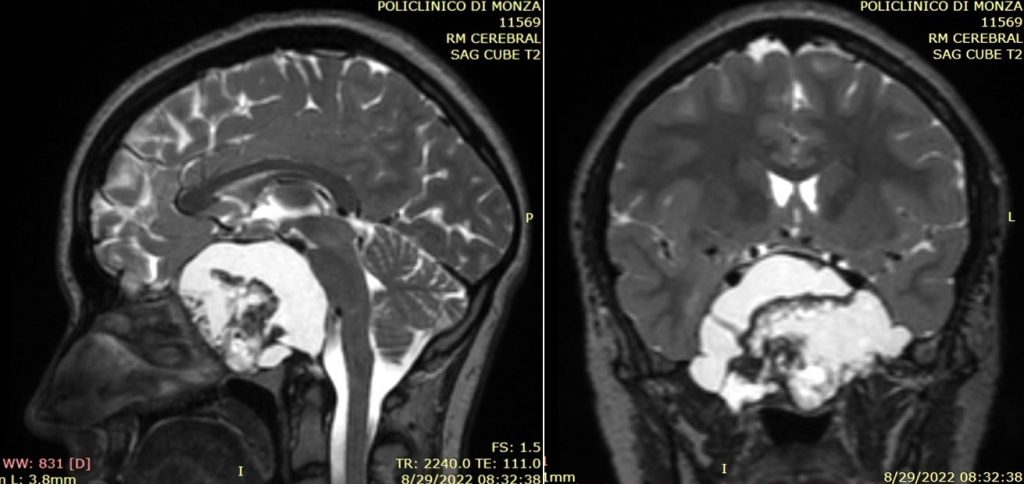
Vă prezentăm în lucrarea de față cazul unei paciente în varstă de 16 ani, investigată imagistic recent pentru diplopie remisă spontan după o evoluție de 4 saptamani. Examenul RMN cu substanță de contrast identifică o masă tumorală cu conținut mixt solid-lichid, cu calcificări și gadolinofilie heterogenă, dezvoltată la nivelul sinusului sfenoid, cu infiltrarea clivusului și extensie spre fosele pterigopalatine bilateral. Formațiunea deplasează cranial și anterior loja și conținutul selar, cu minim contact opto-chiasmatic. Dimensiunile tumorii: 62/66/56 mm. Bilanț hormonal normal.
Examenul radiologic coroborat cu cel neurologic și neurochirurgical stabilesc diagnosticul prezumptiv de craniofaringiom, tip periferic supraselar (fig. 1 a,b)
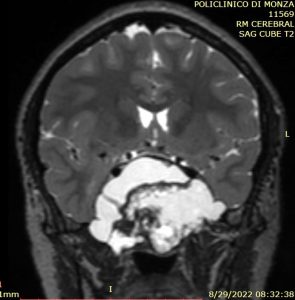
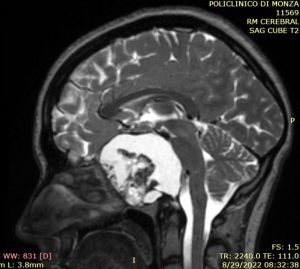
Fig. 1 a,b: RMN preoperator, plan sagital / coronal
Se intervine chirurgical prin abord endoscopic transnazal mononarinar – fosa nazală dreaptă, transsfenoidal, ghidat imagistic cu ajutorul neuronavigației Medtronic Stealth Station, echipă mixtă NCH – Dr. Sergiu Stoica, ORL- Dr. Bogdan Mocanu. Se practică ablația rostumului sfenoidal și se decelază la acest nivel o formațiune tumorală cu consistență mixtă lichidă și solidă, cu zone solide de consistență moale, asociind calcificări. Tumora infiltrează și erodează clivusul în jumătatea superioară până la nivelul durei mater și se extinde lateral bilateral până la nivelul foselor pterigopalatine.
Tips and tricks: debulkingul tumoral creează loc pentru disecţia tumorală extracapsulară ulterioară.
Disecția fină a planurilor arahnoidiene cu instrumente ascuțite/ carlig cu bilă, este critică pentru a evita lezarea ramurilor fine ale arterei hipofizare superioare care alimentează chiasma optică.
O mică parte din podeaua ventriculului 3 poate fi infiltrată tumoral, în acest caz ea ar trebui să fie considerată parte a capsulei tumorale și dacă este posibil – rezecată. Cu toate acestea, hipotalamusul și țesutul cerebral adiacent trebuie conservat și în acest sens, dacă este necesar, un mic rest capsular rezidual aderent poate fi conservat pe pereții ventriculului trei.
În cazul prezentat, s-a practicat chiuretajul și debulkingul tumorii extradurale până la identificarea durei mater clivale, cu menținerea integrității acesteia. Tumora infiltrează planșeul selar, ascensionând conținutul selar. Rezecție tumorală completă, cu frezarea porțiunilor osoase periferice de la nivelul clivusului, cu expunere de țesut osos cu aspect și consistență normale, fără afectarea etanșeității durale. Hemostază și plombaj cu Surgicel. Piesa de rezecție se trimite pentru examen HP/IHC. Fără tamponament nazal.
Evoluție postoperatorie favorabilă, examen neurologic nemodificat, în limite normale, afebrilă. Mobilizare precoce. Fără rinolicvoree. Bilanț hormonal normal. Examinarea RMN cerebrală de control cu substanță de contrast efectuată la 24h postoperator confirmă gradul rezecției. Fără colecții hematice, fără acumulări LCR la nivelul cavității de rezecție.
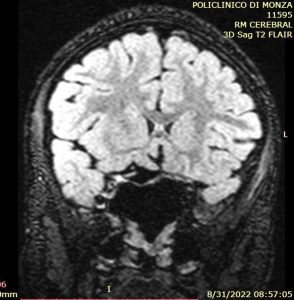
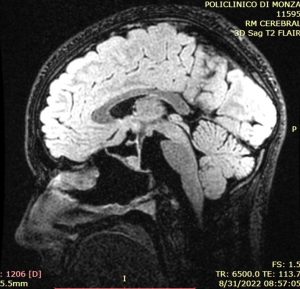
Fig. 2 a,b: RMN la 24h postoperator, plan sagital / coronal
In concluzie: abordul endonazal endoscopic a devenit o tehnică chirurgicală de elecție în zilele noastre pentru managementul craniofaringioamelor. Această metodă oferă un coridor excelent pentru craniofaringioamele de linie mediană infra- și supradiafragmatice. Vederea panoramică oferită de endoscopie și utilizarea opticilor angulate permit îndepărtarea leziunilor care se extind până în cel de-al treilea ventricul, evitând lezarea țesuturilor din vecinătate.
Bibliografie:
- Bin Tang, Shen Hao Xie, Li Min Xiao, Guan Lin Huang, Zhi Gang Wang, Le Yang, A novel endoscopic classification for craniopharyngioma based on its origin, Nature / Scientific Reports, (2018) 8:10215
- de Divitiis, E., Cavallo, L. M., Cappabianca, P. & Esposito, F. Extended endoscopic endonasal transsphenoidal approach for the removal of suprasellar tumors: Part 2. Neurosurgery60, 46–58; discussion 58–59 (2007).
- Gardner, P. A. et al. Outcomes following endoscopic, expanded endonasal resection of suprasellar craniopharyngiomas: a case series. J Neurosurg109, 6–16 (2008).
- Kassam, A. B. et al. Expanded endonasal approach, a fully endoscopic transnasal approach for the resection of midline suprasellar craniopharyngiomas: a new classification based on the infundibulum. J Neurosurg108, 715–728 (2008).
- Komotar, R. J., Starke, R. M., Raper, D. M., Anand, V. K. & Schwartz, T. H. Endoscopic endonasal compared with microscopic transsphenoidal and open transcranial resection of craniopharyngiomas. World Neurosurg77, 329–341 (2012).
- Leng, L. Z., Greenfield, J. P., Souweidane, M. M., Anand, V. K. & Schwartz, T. H. Endoscopic, endonasal resection of craniopharyngiomas: analysis of outcome including extent of resection, cerebrospinal fluid leak, return to preoperative productivity, and body mass index. Neurosurgery70, 110–123; discussion 123–124 (2012).
- Lubuulwa, J. & Lei, T. Pathological and Topographical Classification of Craniopharyngiomas: A Literature Review. J Neurol Surg Rep77, e121–127 (2016).
- Matsuo, T., Kamada, K., Izumo, T. & Nagata, I. Indication and limitations of endoscopic extended transsphenoidal surgery for craniopharyngioma. Neurol Med Chir (Tokyo)54, 974–982 (2014).
- Pascual, J. M., Prieto, R., Carrasco, R., Castro-Dufourny, I. & Barrios, L. Letters to theEditor: craniopharyngioma adherence to the hypothalamus. Neurosurg Focus37, 1–7 (2014).
- Pettorini, B. L. et al. The role of inflammation in the genesis of the cystic component of craniopharyngiomas. Childs Nerv Syst26, 1779–1784 (2010).
- Prieto, R. et al. Craniopharyngioma adherence: a comprehensive topographical categorization and outcome-related risk stratification model based on the methodical examination of 500 tumors. Neurosurg Focus 41, E13 (2016).