Dr. Bogdan Mocanu, Dr. Sergiu Stoica
Prima raportare a unei intervenții chirurgicale transnazale transsfenoidale a fost în 1907, când Schloffer a descris ablația cu succes a unei tumori hipofizare printr-o incizie externă în șanțul labial stâng, lăsând însă cicatrici majore pentru că piramidă nazală a fost dislocata în lateral pentru asigurarea accesului.
Pentru prima data transnazal transseptal (exclusiv endonazal) a intervenit chirurgical otorinolaringologul Oskar Hirsch din Viena, în 1910. Cushing a perfecționat tehnica, introducând abordul sublabial (utilizat încă în multe centre chirurgicale până în zilele noastre) și a efectuat între 1910 și 1925 cu anestezie generală – 231 de intervenții, cu o rată a mortalității de numai 5,6%.
În 1967 Jules Hardy din Montreal a utilizat pentru prima data microscopul pentru abordul transnazal transsfenoidal. În istoria chirurgiei bazei craniului trebuie menționat și chirurgul turc Gazi Yasargil, ulterior apreciat că și neurochirurgul secolului XX pentru contribuțiile sale spectaculoase în vizualizarea microscopica intraoperatorie și localizarea neuroimagistica.
Mai târziu, după ce Wigand, Messelklinger, Stammberger și Kennedy au pus în practică utilizarea chirurgiei nazale endoscopice pentru a diagnostica și a trata leziunile în jurul sinusurilor craniene, la Universitatea din Pittsburg otorinolaringologistul Carrau împreună cu neurochirurgul Kassam în 1997 au raportat experiența lor în abordul tumorilor hipofizare în primele 50 de operații exclusiv endoscopice transnazale. Kassam și Carrau sunt considerați echipa de aur a secolului XXI în abordul rinoneurochirurgical. Alți chirurgi cum ar fi Divitiis, Cappabianca, sunt și ei nume sonore în această lume exclusivista a chirurgiei bazei craniului.
În capitolul de față vom trata afecțiunile cele mai frecvent întâlnite: adenomul hipofizar, craniofaringiomul, cordomul de clivus. Abordul chirurgical se face în aproape toate cazurile în echipă mixtra – neurochirurgie + ORL (exceptie: cordomul de clivus, vezi mai jos). Se creează culoarul chirurgical transnazal mononarinar de către ORL-ist, se incizează dură mater și din acel moment în echipă chirurgicală se alătura neurochirurgul, 3-4 hands surgery până la rezecția completă a tumorii. Închiderea durei mater teoretic cade în sarcină chirurgilor ORL dar în unele cazuri selectate se face tot în echipă mixtă, în situațiile în care sunt necesare manevre complexe cu potențial de lezare a structurilor anatomice din spatele durei (ACI, sinus cavernos, chiasma optică).
ADENOMUL HIPOFIZAR:
Definiție: tumoră benignă cu origine în celulele hipofizei, secretant sau nesecretant de hormoni hipofizari, poate fi microadenom (sub 1cm) sau macroadenom, ca și localizare poate fi intraselar sau cu extensie supra sau paraselară.
Caz clinic 1: macroadenom hipofizar nesecretant: K.A. pacient de sex masculin, 33 de ani, debutul simptomatologiei: sincopa și tulburări vizuale apărute în urmă cu 3 săptămâni, cefalee intensă. La examenul RMN se descoperă o tumoră hipofizara cu un diametru de 38mm, cu invazia sinusului cavernos stâng (fig. 1).
Se decide și se practică abord endoscopic transnazal mononarinar prin fosa nazală stângă, paraseptal. Ablația rostrumului sfenoidal, deschiderea planșeului sellar cu pensa Kerrison de 3mm, incizia orizontală arcuata în “U” inversat a durei mater, ablația de tip piece-meal a tumorii hipofizare sub vizualizarea opticii de 00 și 700. Exereză completă, diafragma sellara etanșă la manevrele Valsalva, fără rinolicvoree, este necesară umplerea cavității de evidare cu material hemostatic. Se poate utiliza material hemostatic din celuloză oxidata regenerată (tip Surgicel), sau pe bază de collagen (Avitene). Se poate introduce in cavitate și burete resorbabil din gelatină (Gelaspon) dar trebuie să ne asigurăm că acesta nu este în contact cu structurile optice (chiasmă, nerv optic) pentru că își poate crește volumul prin acumulare de lichid (sânge, LCR) și poate în acest fel să comprime structurile din jur.
La 24 de ore postoperator se verifică gradul de rezecție prin RMN sau CT cu substanță de contrast (de elecție – RM). De asemenea, în cazul macroadenoamelor nesecretante este obligatoriu RMN de control la 3 luni, 1 an și 2 ani postoperator (fig. 2).
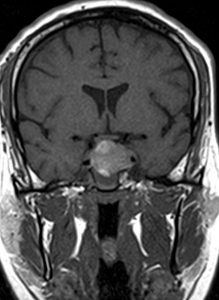
Fig. 1: K.A. macroadenom hipofizar nesecretant cu invazia sinusului cavernos stâng
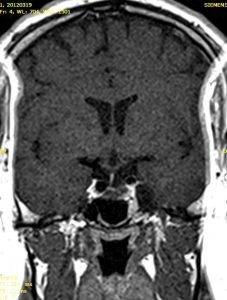
Fig. 2: K.A – control postoperator la 1 an
Analiză imunohistochimica a țesutului tumoral rezecat: GH, TSH, PRL – negative în celulele tumorale. Ki67 – pozitiv cu index nuclear de 1%. Diagnostic histopatologic și imunohistochimic: adenom hipofizar inactiv hormonal, cod ICD – O 8272/0.
Caz clinic 2: microadenom hipofizar secretant de ACTH – Boală Cushing. T.S., pacientă de sex feminin, 57 de ani, obezitate tronculara, vergeturi, hirsutism, “ceafa de bizon”, disfuncții cognitive, iritabilitate, anxietate, insomnie. Examen RMN: formațiune tumorala la nivelul lojei hipofizare în contact cu ACI dreaptă, diametrul orizontal: 6mm, diametrul verical: 4mm.
Testul de supresie overnight cu 1 mg de dexametazona stabilește diagnosticul de boală Cushing.
Se intervine chirurgical endoscopic mononarinar paraseptal (nara dreaptă, de partea leziunii). Ablația rostrumului sfenoidal, deschiderea planșeului sellar cu freza diamantata de 2mm, incizia durala în “U” inversat. Se descoperă formațiunea tumorala gri-cenușie, cu o limită clară de demarcație față de țesutul hipofizat normal. Rezecția în bloc a formațiunii, inspecția cavității restante cu optică de 00 – fără fistulă LCR la finalul intervenției (diafragma selara etanșă).
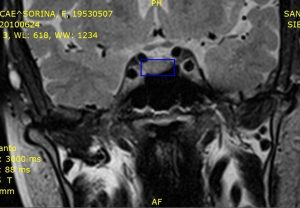
Fig. 3: T.S. microadenom hipofizar secretant de ACTH, în contact cu ACI dr.
Cortizolemia la 24h postoperator – la limită inferioară a valorilor normale.
Analiză imunohistochimica a țesutului tumoral rezecat: ACTH-pozitiv cu intensitate variabila în celulele tumorale, Ki 67-pozitiv cu index nuclear 1%, Synaptophysin-pozitiv în celulele tumorale, diagnostic histopatologic și imunohistochimic: adenom hipofizar corticotrop, cod ICD-O 8272/0.
CRANIOFARINGIOMUL:
Definiție: tumoră disembrioplazica, cu origine în resturi ale pungii lui Rathke. Reprezintă 1-3% din toate tumorile cerebrale, originea o găsim de regulă în tijă hipofizara în regiunea supraselara, adiacent de chiasmă optică. Particularitatea acestor tumori: în urmă unei rezecții complete întotdeauna la finalul intervenției avem o fistulă LCR cu debit mare pentru că tumora se rezeca în bloc cu tija hipofizară, în acest fel rămâne o breșă largă în diafragma selara.
Caz clinic: pacientul P.C. de sex masculin, în vârstă de 38 de ani, se prezintă la spital pentru tulburări vizuale (PMM-OS, ND-OD), sindrom cefalalgic sever neresponsiv la tratament analgezic, panhipopituitarism, diabet insipid.
Examenele radiologice pun în evidența o tumoră cu originea la nivelul lojei hipofizare, extinsă paraselar, diametrul vertical 80mm, cu o porțiune chistica la polul superior. Formațiunea înglobează complexul arterial cerebral anterior, invadează ventriculul 3 și ventriculii laterali (fig. 4).
Se intervine chirurgical endoscopic transsfenoidal mononarinar drept. Tumora are o consistență variabila, cu numeroase calcificări și un înveliș fibros aderent la structurile din jur. La polul superior găsim porțiunea chistica ce conține un lichid cu aspect de “ulei ars de motor”, caracteristic craniofaringioamelor.
Rezecție macroscopic completă, fistula LCR se închide multistrat cu țesut adipos fixat cu adeziv biologic (se poate utiliza soluție care are la bază polietilen glicol – Duraseal, adeziv din fibrină – Tissucol sau adeziv acrilic – Ifabond) și un al doilea strat de țesut adipos și material hemostatic (Surgicel), fixate cu o grefa de os recoltata inițial din rostrumul sfenoidal, așezată underlay sub rebordul osos al planșeului sellar.
RMN de control cu substanță de contrast la 24h postoperator – confirmă gradul de rezecție tumorala (fig. 5).
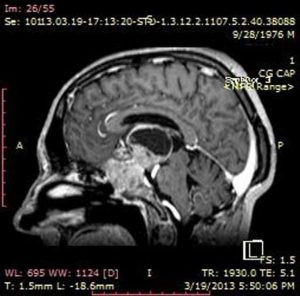
Fig. 4: P.C. craniofaringiom cu diametrul vertical de 80mm, porțiune chistica la polul superior, calcificări intratumorale specifice
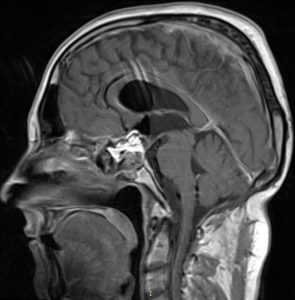
Fig. 5: P.C.-control postoperator la 24: fără restanța tumorala, lojă ocupată cu material hemostatic și țesut adipos.
Examenul HP și IHC: fragmente tisulare reprezentate de arii întinse de necroza, calcificări și cristale de colesterol cu numeroase celule gigante multinucleate, țesut fibroconjunctiv cu infiltrat inflamator cronic și hemoragie. Ki 67-pozitiv nuclear în celule foarte rar. Diagnostic histopatologic și imunohistochimic: craniofaringiom
CORDOMUL DE CLIVUS
Definiție: tumoră embrionara dezvoltată din resturi embrionare sau malformații preexistente, localizată mai frecvent în regiunea sacrococigiana și destul de rar în zonă sfenooccipitala. Cordomul de clivus are potențial de transformare maligna, cu evoluție fulminantă în bază craniului. Conduita terapeutică modernă constă în ablația chirurgicală și protonterapie postoperator. Fiind o tumoră dezvoltată extradural, această patologie poate fi rezolvată chirurgical exclusiv prin echipă operatorie ORL.
Caz clinic: paciență I.R. de sex feminin, 58 de ani, sindrom cefalalgic sever, amputație de câmp vizual, afectare multiplă a nervilor cranieni și hipertensiune intracraniana. Examenul CT/RMN descrie o formațiune tumorala cu un diametru vertical de 76mm, care erodează si invadează structura osoasă a clivusului și se extinde paraclival în toate direcțiile, inferior până la atlas și procesul odontoid al axisului, superior până la clinoidele anterioare, cu efect de masă asupra trunchiului cerebral și protruzionand în rinofaringe. Formațiunea ocupă în totalitate sinusul sfenoid (fig.6).
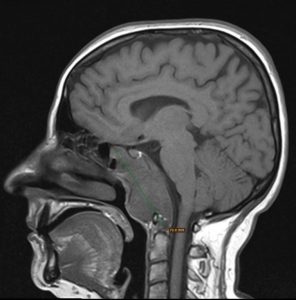
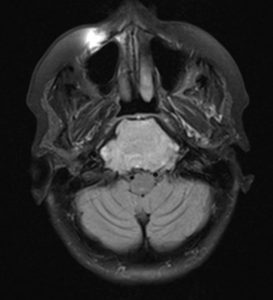
Fig. 6: examen RMN sagital și axial preoperator
Planul de rezecție chirurgicală a inclus 3 etaje: transnazal transsfenoidal, transnazal transrinofaringian și transoral (fig.7). Operația debutează cu un abord transrinofaringian, un flap de mucoasă realizat prin incizia in “U” inversat cu laturile verticale în foseta Rosenmuller și latura orizontală superioară la joncțiunea dintre tavan și peretele posterior al rinofaringelui. Se rabatează acest flap în direcția orofaringelui și în acest fel avem un abord larg asupra poțiunii mijlocii și inferioare a cordomului.
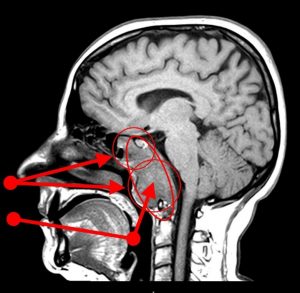
Fig. 7: Planul de abord chirurgical
Un depărtător autostatic bucal asigură introducerea transorală a unor instrumente angulate în câmpul operator (aspiratoare angulate, pense Heuwieser de 900 și 1200) iar abordul transsfenoidal deschide calea către polul superior al tumorii.
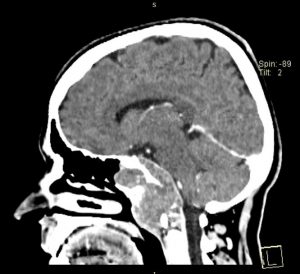
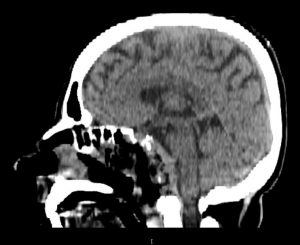
Fig. 8: CT cu substanță de contrast stg. – preoperator, dr.-postoperator la 24h
Formațiunea are o consistență crescută, variabilă – cartilaginoasa cu insule de calcificări; exereza se face cu ajutorul instrumentarului rece, al microdebriderului și sub controlul navigației chirurgicale computerizate.
La finalul operației cavitatea de evidare este încărcată cu țesut adipos recoltat periombilical. Se asigură retentivitatea cavității prin sutura endoscopica a flapului de mucoasă cu fire separate, portacul fiind introdus prin cavitatea orală.
Gradul de rezecție de aproximativ 90% este confirmat radiologic prin CT cu substanță de contrast efectuat la 24h postoperator (fig.8). Pacienta este îndrumată către protonterapie.